Die Elektrolyse von Wasser hat eine lange Geschichte. Britische Chemiker zerlegten bereits im Jahr 1800 erstmals Wasser mit Hilfe des elektrischen Stroms und erzeugten so Wasserstoff und Sauerstoff. Die Umkehrung, das heißt die Reaktion der beiden Gase unter Erzeugung von Elektrizität, gelang rund 40 Jahre später – die Grundlage der Brennstoffzelle.
Zunehmende Bedeutung
Anfang des 20. Jahrhunderts gewann jedoch zunächst der stoffliche Einsatz von Wasserstoff an Bedeutung. Mit dem Haber-Bosch-Verfahren wird seitdem Ammoniak (und schließlich Dünger) aus Wasserstoff und Stickstoff erzeugt. Die großen Mengen Wasserstoff, die dafür nötig waren, wurden mithilfe der Kohlevergasung oder der Dampfreformierung (aus Erdgas und Wasser) erzeugt. Dabei entsteht jeweils auch klimaschädliches Kohlendioxid – im Gegensatz zum Elektrolyse-Verfahren. Elektrolyseure waren jedoch lange nicht leistungsfähig genug, um eine wirtschaftliche und zugleich ökologische Alternative darzustellen.
Vor dem Hintergrund der ersten Ölkrisen in den 1970er und 1980er Jahren kreierten Entwickler die ersten Konzepte, in denen Wasserstoff eine Rolle als Energieträger spielte. In Projekten wie HYSOLAR wurde Wasserstoff mithilfe von Solar-Strom erzeugt. Die Verfahren waren zwar noch weit davon entfernt, wirtschaftlich zu arbeiten.
Es erstaunt dennoch, dass nicht mit Hochdruck an ihrer Optimierung gefeilt wurde. Denn die Endlichkeit fossiler Brennstoffe war bekannt. Und die steigende Kohlendioxid-Konzentration in der Atmosphäre wurde damals bereits von zahlreichen Experten äußerst kritisch bewertet. Immerhin stellten die Hysolar-Partner (Saudi-Arabien und Deutschland) bereits 1994 die weltweit erste technische Wasserstoffproduktion, bei der Photovoltaik und Wasserelektrolyse direkt gekoppelt wurden, vor.
Verschiedene Verfahren der Wasserelektrolyse
Seitdem jedoch mehr und mehr Windkraft- und Photovoltaikanlagen elektrische Energie erzeugen, wird immer deutlicher: Wasserstoff, den man mithilfe von überschüssigem elektrischem grünem Strom erzeugt, wird ein wichtiger Bestandteil der Energiewende werden. Im Rahmen der Sektorenkopplung kann er als Speichermedium dienen.
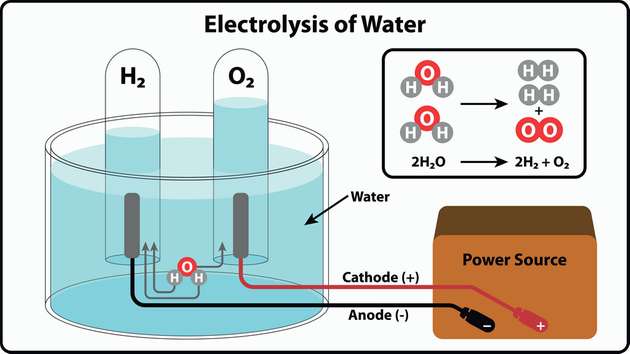
Das denkbar einfache Prinzip der Wasserelektrolyse besteht aus zwei Teilreaktionen, die in saurer Lösung oder alkalischer Lösung unterschiedlich ablaufen. In saurer Lösung entsteht an der Kathode aus Hydronium-Ionen (H3O+) Wasserstoff und Wasser. Und an der Anode wird Wasser zu Sauerstoff und Hydronium-Ionen umgesetzt. In Kalilauge oder mit neutralen Salzen als Elektrolyt wird Wasser dagegen an der Kathode zu Wasserstoff und Hydroxid-Ionen (OH-). An der Anode reagiert Wasser zu Sauerstoff und Hydronium-Ionen.
Die für diese Prozesse genutzten Wasserelektrolyseure enthalten neben Kathode und Anode sowie den Behältern für den Elektrolyten eine Membran (Diaphragma). Sie trennt den Kathoden- und Anodenbereich und verhindert, dass die entstehenden Gase Wasserstoff und Sauerstoff miteinander in Berührung kommen. Dabei lässt sie jedoch selektiv die entstehenden Ionen (H+ bei saurem, OH- bei alkalischem Elektrolyseur) durch. So kann der Stromkreis geschlossen werden.
Inzwischen gibt es diverse Typen von Wasserelektrolyseuren, bei denen mehrere Elektrolysezellen aneinandergereiht werden. Sie unterscheiden sich neben dem eingesetzten Elektrolyten auch im Aufbau der Zellen im Detail (etwa der Membran, der Gasdiffusionsschicht GDL, der Art der Bipolarplatten und der Katalysatoren) und durch die Temperaturen und Drücke, die während der Elektrolyse herrschen. Unterm Strich entstehen in allen Elektrolyseuren unter Einsatz von Gleichstrom aus zwei Wassermolekülen zwei Wasserstoffmoleküle und ein Sauerstoffmolekül.
Folgende Elektrolyseur-Arten sind am verbreitetsten
AEL (alkalische Elektrolyseure): arbeiten meist mit Kaliumhydroxid-Lösung als Elektrolyt und nickelbasierten Elektroden. Alternativ kommen auch Titanelektroden mit einer Beschichtung aus Ruthenium- oder Iridiumoxid zum Einsatz. AEL werden bei Temperaturen zwischen 40 und 90 °C und einem Druck von ein bis 30 bar betrieben. Ein seit der 1950er etablierter Elektrolyseur mit hoher Langzeitstabilität.
PEM (Proton Exchange Membrane, saure Elektrolyseure): arbeiten mit destilliertem oder Trinkwasser. Als Elektrolyt dient eine protonendurchlässige Polymermembran. Sie ist auf der Kathodenseite mit Platin/Kohlenstoff und auf der Seite der Anoden mit Iridium- oder Rutheniumoxid beschichtet. Die Bipolarplatten bestehen aus Titan.
Es gibt auch reversible PEM, die sowohl als Brennstoffzelle als auch als Elektrolyseure arbeiten können. Für den Einsatz zur Energiespeicherung in Kombination mit einem Wasserstoff-Speicher ist dies von Vorteil. Die PEM-Elektrolyseure sind weitgehend wartungsfrei. Im Gegensatz zu AEL können sie innerhalb von Sekunden aus dem Standby auf Volllastbetrieb gefahren werden. Das ist besonders zur Speicherung von Windenergie wichtig.
SOE (Solid Oxide Electrolysis; Feststoffoxid-Elektrolyseure): Elektrolyt ist ein keramischer Werkstoff zwischen den Halbzellen. Wasser wird dampfförmig zugeführt. SOE werden bei 600 bis 900 °C betrieben (Hochtemperaturelektrolyse) und erreichen – unter anderem aufgrund der als Wärme eingekoppelten zusätzlichen Energie – einen hohen Wirkungsgrad von über 80 Prozent.
AEM (Anion Exchange Membrane, Anionenaustauschmembran): enthält eine ionenleitende, auf beiden Seiten mit Katalysator beschichtete Membran. Im Unterschied zur PEM wandern Hydroxidionen (OH-) hindurch. Die Membran des neueren AEM-Elektrolyseurs ist deutlich kostengünstiger als die des PEM-Elektrolyseurs. Sie ist von Gasdiffusionsschichten umhüllt. Den Abschluss auf beiden Seiten bilden Stahl-Bipolarplatten. Der Wirkungsgrad wird mit 62,5 Prozent angegeben. Es entsteht Wasserstoff mit einer Reinheit von 99,9 Prozent.
Gefahren von Wasserstoff sind beherrschbar
Sicherheitstechnisch sind alle Verfahren vergleichbar. Der gebildete Wasserstoff liegt zunächst in Wasser gelöst vor. Falls Elektrolyt austritt, kann Wasserstoff freigesetzt werden. Wasserstoff kann mit dem ebenfalls entstehenden Sauerstoff oder mit der Umgebungsluft ein äußerst explosionsfähiges Gemisch bilden– und das in einem sehr breiten Explosionsbereich. Gemische mit einem Gehalt zwischen 4 und 77 Volumenprozent können explodieren. Dafür ist nur eine sehr geringe Zündenergie von 0,02 mJ nötig. Damit gehört Wasserstoff in die gefährlichste Zündgruppe IIC.
Extrem ist auch die hohe Flammausbreitungsgeschwindigkeit, durch die Wasserstoffexplosionen sehr zerstörerisch wirken. Nicht zuletzt der über 100-jährigen Verwendung von Wasserstoff in der chemischen Industrie ist es zu verdanken, dass diese Gefahren gut bekannt und beherrschbar sind. Heute regeln die Normenreihen IEC 60079 und IEC80079 den Explosionsschutz. Die Anforderungen an den sicheren Bau und Betrieb von Elektrolyseanlagen ist im internationalen Standard ISO 22734 beschrieben.
Primärer Explosionsschutz durch geeignete Bauweise
Naturgemäß steht im Vordergrund, ein explosionsfähiges Gemisch erst gar nicht auftreten zu lassen. Die Dichtigkeit der gesamten Anlage, die verhindert, dass Wasserstoff entweicht, ist eine der wichtigsten Maßnahmen des primären Explosionsschutzes. Gassensoren in der Umgebung würden bereits bei einer sehr geringen Wasserstoffkonzentration Alarm schlagen.
Diesen primären Explosionsschutz zu gewährleisten, ist nicht trivial. Denn Wasserstoffmoleküle sind mit 0,276 nm sehr klein; sie können durch viele metallische Werkstoffe diffundieren. Dabei können Metalle verspröden. Dichte Apparaturen und Rohrleitungsverbindungen sind daher aufwendiger zu realisieren als bei den meisten anderen Prozessen. Insbesondere bei Hochtemperaturverfahren wie der SOE, die bei Temperaturen über der Mindestzündtemperatur (585 °C) von Wasserstoff ablaufen, bestehen hohe Anforderungen. Es muss auch unbedingt verhindert werden, dass der entstandene Wasserstoff durch Sauerstoff verunreinigt werden kann.
Zoneneinteilung und sekundärer Explosionsschutz
Risikoanalysen, die der Anlagenbauer durchzuführen hat, stellen potenzielle Gefahren systematisch dar – und mit ihnen die nötigen Gegenmaßnahmen. Basis für Sicherheit ist die Zoneneinteilung nach IEC 60079-10-1, für die der Betreiber zuständig ist. Nicht nur der Elektrolyseur, sondern auch die folgende Gasaufbereitung, etwaige Verdichter, Rohrleitungen und Speicher sind zu betrachten. Zonen charakterisieren explosionsgefährdete Bereiche in Abhängigkeit von der Dauer und Häufigkeit mit der eine gefährliche explosionsfähige Atmosphäre (g. e. A.) auftreten kann:
Zone 0: Bereich, in dem g. e. A. ständig, über lange Zeit oder häufig vorhanden ist.
Zone 1: Bereich, in dem sich im Normalbetrieb gelegentlich eine g. e. A. bilden kann.
Zone 2: Bereich, in dem im Normalbetrieb eine g. e. A. nicht oder nur selten und für kurze Zeit auftritt.
An der Zoneneinteilung orientiert sich wiederum der sekundäre Explosionsschutz: die Vermeidung von Zündquellen. Ein kritischer Bereich der Zone 2 kann zum Beispiel direkt unter der Decke von Räumen herrschen, in denen Elektrolyseure betrieben werden. Ob der Bereich jedoch tatsächlich so eingestuft werden muss, hängt von weiteren organisatorischen und technischen Maßnahmen ab.
Eine Zwangslüftung an dieser Stelle kann zum Beispiel verhindern, dass sich dort Wasserstoff bis zum kritischen, explosionsfähigen Konzentrationsbereich anreichern kann. Da sich gasförmiger Wasserstoff sehr schnell verflüchtigt, reicht dies in der Regel aus, um das Explosionsrisiko zu minimieren. Auf eine Zone kann dann verzichtet werden.
Unterschiedliche Konzepte für Nieder- und Hochdruck-Elektrolyseure
Dies ist in der Regel bei atmosphärischen Elektrolyseanlagen bis 50 mbar Betriebsdruck der Fall, sofern nur äußerst geringe Wasserstoffmengen austreten können. Durch regelmäßige Kontrollen und etwaigen Austausch von Komponenten wie etwa Dichtungen muss dies auf Dauer gewährleistet werden. Zudem sichern Gaswarneinrichtungen den sicheren Zustand ab beziehungsweise warnen, sobald die Raumatmosphäre unzulässig durch Wasserstoff verunreinigt wird.
Bei Druckelektrolyseanlagen, die bei bis zu 100 bar Betriebsdruck arbeiten, sind derartige Gaswarneinrichtungen besonders wichtig. Sie müssen gegebenenfalls die Anlage frühzeitig abschalten. Als Zone 2 ist hier meist ein Bereich von jeweils 0,5 m um den Zellenblock und bis zur Decke eingestuft. Hochdrucksysteme sind energetisch günstig, erfordern aber die genau Kenntnis der Druck- und Temperaturabhängigkeit von Explosionsgrenzen des Wasserstoff-Sauerstoff-Systems.
Auch Permeations- und Leckraten sind von Experten sorgfältig zu ermitteln. Der Elektrolyseur muss so betrieben werden, dass gefährliche Verunreinigungen des Wasserstoffs durch Sauerstoff – etwa durch eine fehlerhafte Trennung der Gase im Prozess – vermieden wird.
ATEX-zertifizierte Betriebsmittel in Zone 0 bis Zone 2
In Bereichen, die in Zone 0 bis Zone 2 eingestuft sind, dürfen selbstverständlich nur geeignete, entsprechend zertifizierte Betriebsmittel eingesetzt werden. Portable Geräte sollten idealerweise für Zone 0 geeignet sein. Dies bringt maximale Sicherheit, auch wenn sich Mitarbeiter bei Anlagenbegehungen regulär nur in Zone 2 aufhalten sollten.
Bedienpanels für Zone 1 und Zone 2 sowie explosionsgeschützte Schalttafeln mit Ex-d- oder Ex-e-Gehäuse können nahe der Elektrolyseure installiert werden. Auch Relaismodule und Messumformer-Speisegeräte sollten über eine entsprechende ATEX-Zulassung für Zone 1 oder 2 verfügen. Die Schaltschränke können zudem mit einem Belüftungssystem ausgerüstet werden, das die Anreicherung von Wasserstoff bis in den kritischen Bereich verhindert.
Kompletter Explosionsschutz für Gigawatt-Anlagen
Bei der Erzeugung von Wasserstoff gelten strenge Regeln. Je nach Bau- und Betriebsart der Elektrolyseure sowie der weiteren Anlagen des Wasserstoffsystems ergeben sich spezielle Anforderungen an den primären, sekundären und tertiären Explosionsschutz. Auch Pumpen zur Zuführung von Wasser und/oder Elektrolyt, Gastrockner und vieles mehr müssen den hohen Sicherheitsanforderungen genügen.
Darüber hinaus ist sicherzustellen, dass die eingesetzten Produkte für die Stromversorgung und die Steuerung der Anlagen sowie etwaige Ventilatoren, Leuchten, Sensoren und vieles mehr jederzeit sicher betrieben und ein eventuell auftretendes Wasserstoff-Luft-Gemisch nicht entzünden können. Elektrolyseanlagen, die sich auf dem Weg zur Massenfertigung befinden, müssen besonders sorgfältig konzipiert werden. Neben dem Faktor Sicherheit gilt es auch, ihre Zuverlässigkeit zu optimieren.
So können künftig Gigawatt-Anlagen in Modulbauweise entstehen, die einen maßgeblichen Beitrag zur sicheren Energieversorgung mit grünen klimaneutralen Technologien leisten.




.jpg)