Elektrochemische und materialwissenschaftliche Einflüsse auf die Energiedichte von elektrochemischen Speichern sind in der Literatur bereits umfänglich beschrieben. Für verfahrenstechnische Voraussetzungen gilt dies jedoch weniger [1]. Grundsätzlich unterscheidet sich die Konstruktionsaufgabe nicht von Brennstoffspeichern, bei denen Brennstoffzellen elektrische Arbeit elektrochemisch erzeugen. Analog zu Wasserstoff (H2) wird das Speichervolumen dabei auf zwei Arten bestimmt:
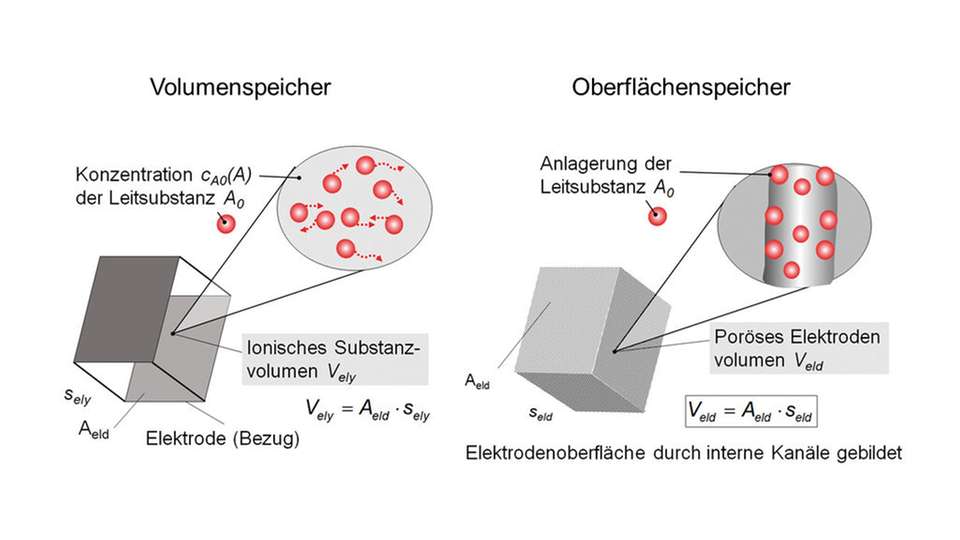
Bei der Volumenspeicherung entspricht das Speichervolumen der Anodenseite dem Volumen der elektronenliefernden Substanz, zum Beispiel H2. Bei deren Anlagerung an porösen Oberflächen wie Metallhydridspeicher bei H2 folgt das Speichervolumen aus den Volumina des porösen Speichermaterials, der zugehörigen Hohlräume und der an der Oberfläche angelagerten Substanz. Die volumenbezogene spezifische Oberfläche (SV) bestimmt wesentlich das Aufnahmevermögen.
Bei elektrochemischen Speichern werden anstelle von H2 meist andere Substanzen wie etwa Lithium (Li), Vanadium (V) und Natrium (Na) verwendet. Die Abbildung auf Seite 70 oben links stellt die Volumen- und die Oberflächenspeicherung gegenüber. Der linke Teil der Abbildung zeigt die Volumenspeicherung. Sie ist charakteristisch für Natrium-Schwefel-Batterien (kurz NaS-Batterien). Die Oberflächenspeicherung wie rechts in der Abbildung dargestellt, kommt beispielsweise bei Lithium-Ionen-Batterien vor.
Batteriegeometrie und Energiedichte
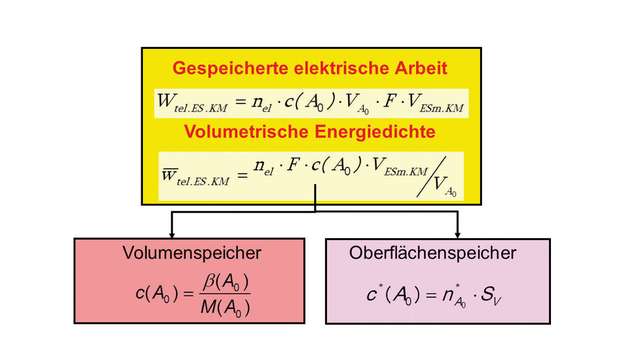
Die Einflüsse der Speichergeometrie auf die abgebbare elektrische Arbeit Wtel.ES.KM und die volumetrische Energiedichte w̅tel.ES.KM der elektronenliefernden Leitsubstanz A0 (analog zu Brennstoffen) fasst die Abbildung auf Seite 70 oben rechts zusammen.
Bei Volumenspeichern hängt die Stoffmengenkonzentration c(A0) von der Massenkonzentration β(A0) und der Molmasse M ab. Bei Oberflächenspeichern dagegen hängt die Stoffmengenkonzentration von der oberflächenbezogenen Stoffmenge nA0* und der spezifischen Oberfläche SV ab, nA0* folgt aus dem Partikeldurchmesser von A0.
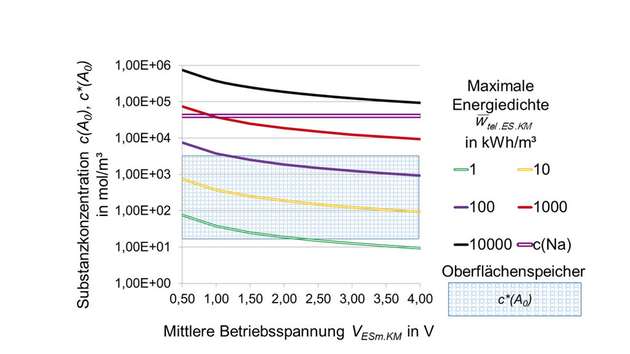
Die volumetrische Energiedichte W̅tel.ES.KMhängt neben der Elektronenzahl nel nur von c(A0), der mittleren Entladungsspannung VESm.KM und der Faradaykonstanten F ab. Die Abbildung auf Seite 71 oben links zeigt diese Abhängigkeit für nel = 1. Die Darstellung verdeutlicht zudem die Einflüsse auf die Energiedichte durch die Prozesskoordinaten c(A0) und die mittlere Betriebsspannung bei Entladung VESm.KM. Beide sind eine Konsequenz der gewählten elektrochemischen Reaktionen, des Speicherverfahrens sowie gegebenenfalls von SV. Die Reaktionen der Kathodenseite müssen zur Entwicklung des Diagramms nicht betrachtet werden, da sie nur die Variable VESm.KM beeinflussen.
Das Volumen der Kathodenseite kann analog bestimmt werden und ist bei luftbetriebenen Systemen gleich null. Bei von 1 abweichender Elektronenzahl ist das Ergebnis mit nel zu multiplizieren [1]. Mit Literaturwerten [1] für SV und möglichen Moleküldurchmessern folgt der eingezeichnete Bereich von c(A0)* für die Oberflächenspeicherung. Deren potenzielle Speicherdichte liegt somit etwa um den Faktor 10 unter der von Volumenspeichern, siehe c(Na).
Batch- und Fließprozesse
Sowohl Volumen- als auch Oberflächenspeicher werden als Batchprozesse ausgeführt und das Inventar der Speicher ist durch die Batteriegeometrie begrenzt. Die Volumenspeicherung erlaubt bei einer Lagerung der Reaktanden in getrennten Tanks ein nahezu beliebiges Speichervolumen. Davon getrennt erfolgt die elektrochemische Reaktion im Zellstack.
Dieses Konzept der Redox-Flow-Batterie (RFB) reduziert auch die Brandgefahr, weil das Inventar im Stack beschränkt bleibt. Allerdings werden bei vielen heutigen RFB-Entwicklungen Lösungen mit recht geringen Werten von c(A0) verwendet. Deshalb wurde im Rahmen eines Seminarprojekts am Institut für Energiesysteme und Brennstoffzellentechnik an der HAW Hamburg die prinzipielle Eignung der NaS-Batterie für das RFB-Verfahren untersucht [2].
Wesentliche Ergebnisse dieser Konstruktionsstudie waren der Nachweis der prinzipiellen Machbarkeit und der in der Abbildung auf Seite 71 oben rechts gezeigte Vorteil von RFB im Grundflächenbedarf.
NaS-Batterien werden bereits eingesetzt. Zudem sind sowohl flüssiges Natrium (thermische Solarkraftwerke, schneller Brüter) als auch flüssiger Schwefel (Chemieindustrie) in Fließprozessen zum Einsatz gekommen. Aus diesem Grund ist das Entwicklungsrisiko für Großspeicher überschaubar.
Fazit
Das Gelingen der Energiewende benötigt sowohl die Leistungsspeicherung vor allem zur Rekuperation als auch die umfängliche Speicherung elektrischer Arbeit als Reserve. Die Oberflächenspeicherung eignet sich besonders zur Bereitstellung von Leistung, während die Volumenspeicherung vorzugsweise als Redox-Flow-Batterien der Bereitstellung von Arbeit dient.
Eine angestrebte Technologieführerschaft erfordert also auch eine klare verfahrenstechnische Ausrichtung der Forschungs- und Entwicklungsstrategie.
Weitere Informationen
[1] W. Winkler: Process Engineering Considerations of Electrochemical Storage. Journal of Energy and Power Engineering 8 (2014) 1763-1776
[2] P. Lorenzen, J. Dinter: Natrium-Schwefel-Flussbatterie. Projektarbeit am Institut für Energiesysteme und Brennstoffzellentechnik, HAW Hamburg. 2012







.jpg)







